
Nature Communications|吴华君/徐明团队开发跨尺度三维基因组预测深度学习框架Hi-Compass
2026年4月14日,北京大学临床医学高等研究院(细胞稳态与衰老性重大疾病北京研究中心)/北京大学肿瘤医院吴华君、北京大学第三医院徐明和北京大学肿瘤医院王玉娟共同通讯在 Nature Communications 上发表了题为 "Hi-Compass: a depth-aware deep learning framework for predicting cell-type-specific 3D genome organization from single-cell to spatial resolution" 的研究论文。该工作提出了深度学习框架Hi-Compass,以ATAC-seq数据为唯一的细胞类型特异性输入,实现了从bulk到单细胞、再到空间分辨率的跨尺度Hi-C接触图谱预测。

基因组的三维空间折叠决定了远端调控元件与靶基因之间的物理接触,是细胞类型特异性基因表达调控的重要结构基础【1–3】。Hi-C技术的发展使研究者能够在全基因组范围内解析染色质互作图谱,揭示了compartment、TAD和染色质环等多层次三维结构及其在发育与疾病中的功能意义【4,5】。然而,高分辨率Hi-C实验对测序资源要求极高,在单细胞和空间组学等新兴数据类型中获取可靠的三维基因组信息仍是一项重大挑战。
已有的深度学习预测方法(如Akita、C.Origami、Epiphany、ChromaFold等)在一定程度上缓解了实验瓶颈,但在面向单细胞和空间数据时仍受限于多组学配套需求、跨细胞类型泛化不足以及对数据稀疏性的适应能力有限等问题。
作者团队提出的Hi-Compass模型采用CNN-Transformer架构,整合ATAC-seq信号、DNA序列、泛细胞类型CTCF结合谱和测序深度四类输入。针对不同实验平台间测序深度差异悬殊的问题,作者在训练中纳入多种深度的ATAC-seq数据,并通过**深度嵌入(depth embedding)**编码输入深度信息,使模型适应从高覆盖bulk到极度稀疏单细胞的全谱数据。
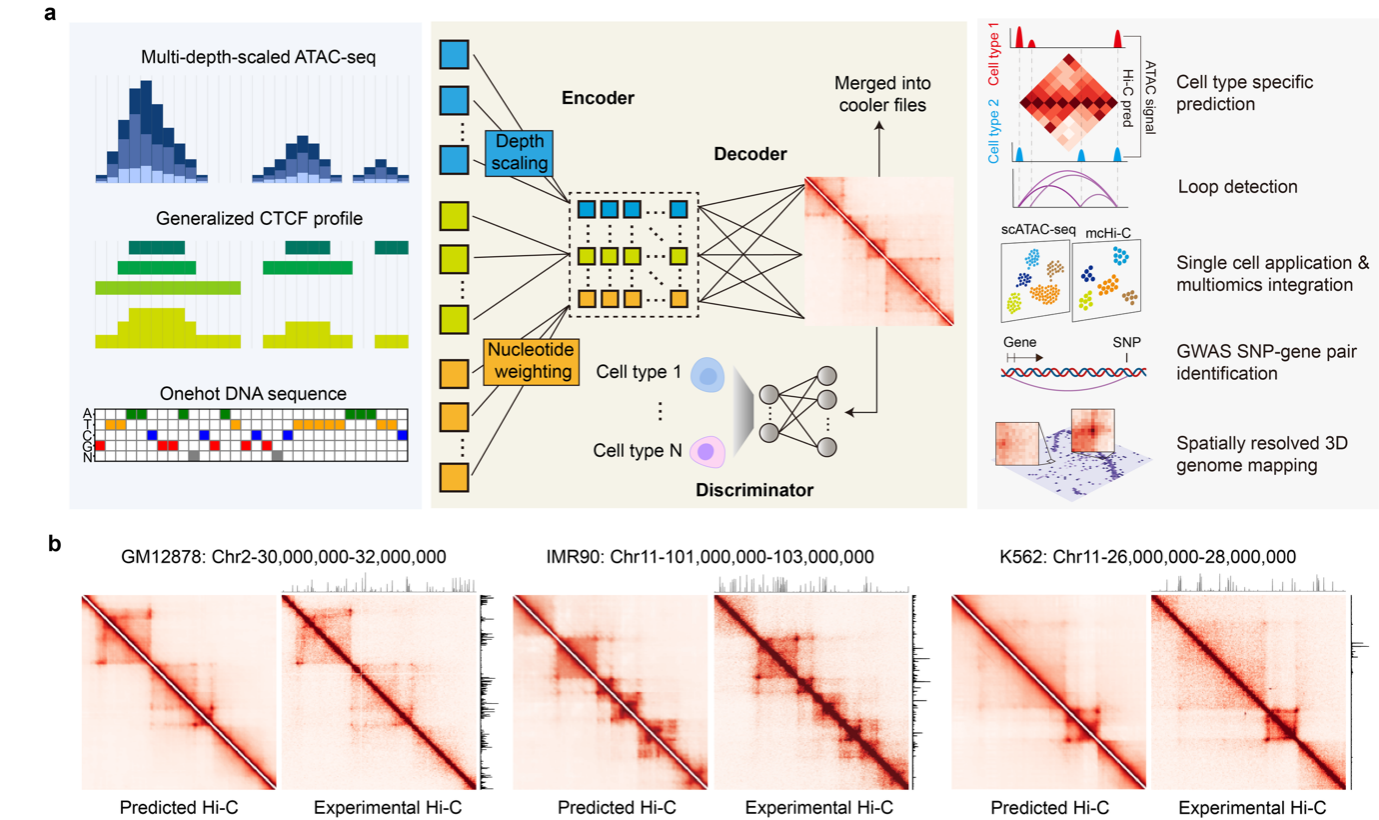
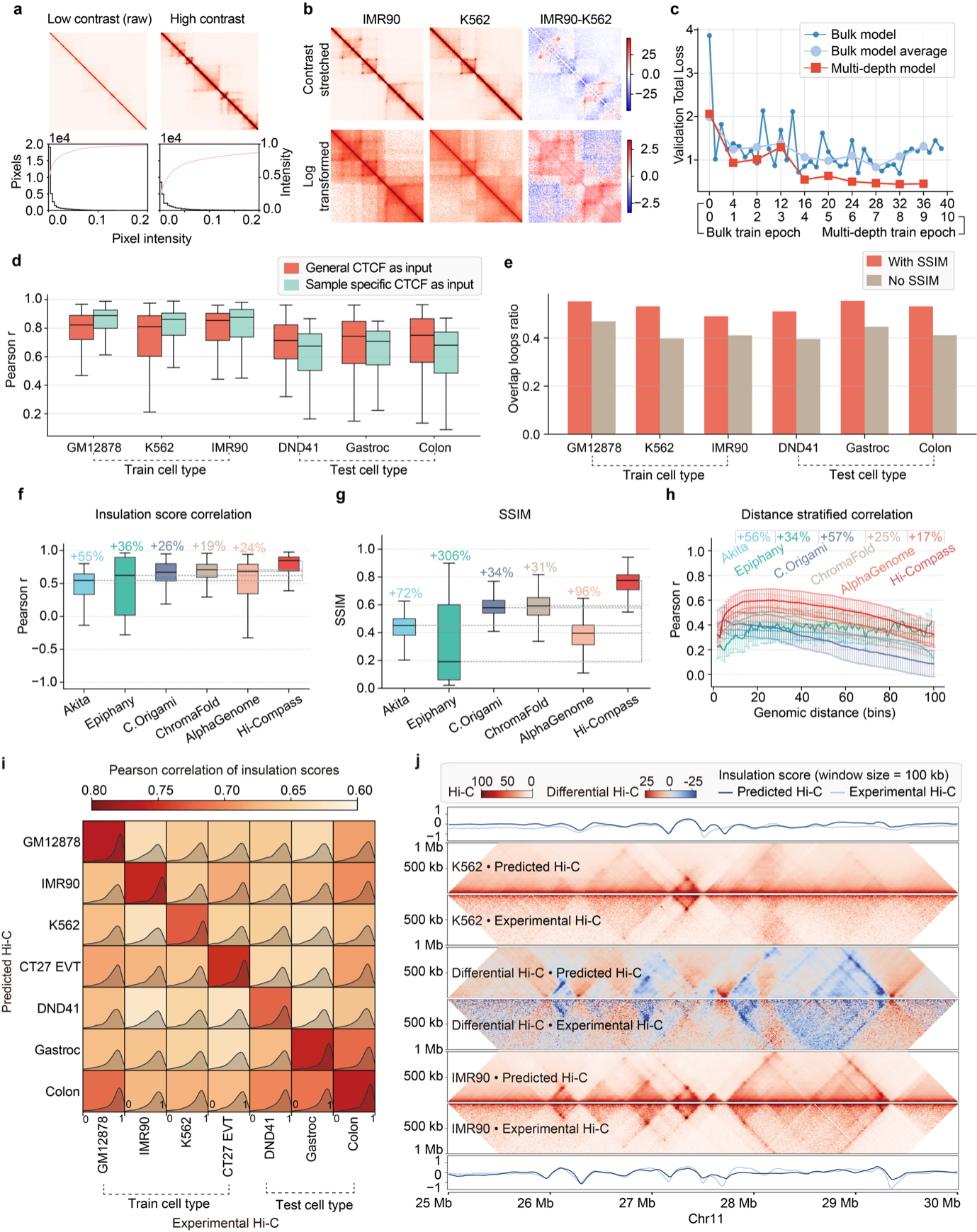
系统性benchmark显示,Hi-Compass在Hi-C图谱相关性、染色质环恢复及insulation score一致性等指标上优于Akita、C.Origami、Epiphany和ChromaFold等方法,尤其在跨细胞类型泛化场景中表现突出。结合多细胞类型联合训练,Hi-Compass对训练集之外的细胞类型同样具备zero-shot预测能力。
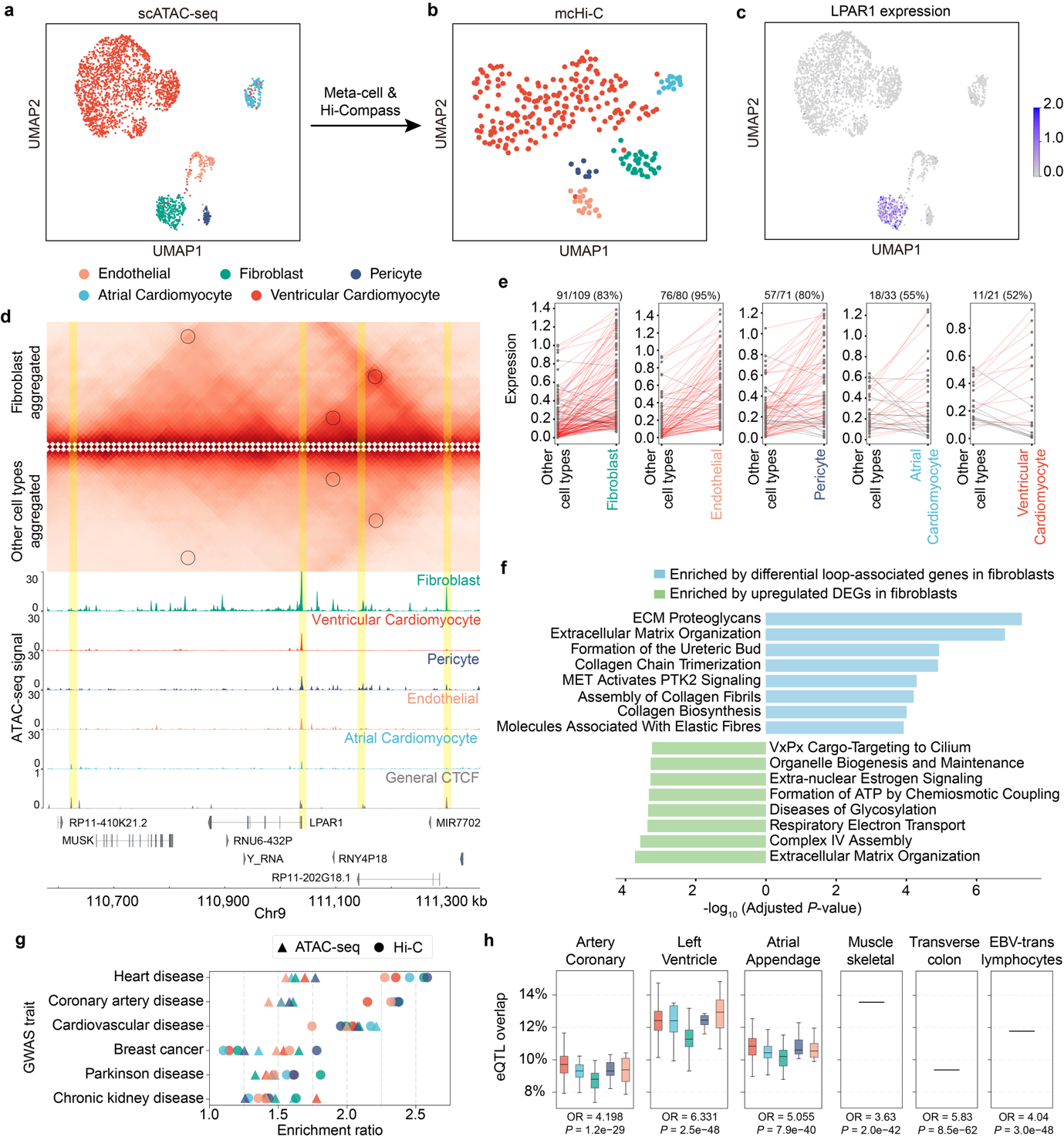
在应用层面,作者将Hi-Compass分别应用于PBMC scATAC-seq和胚胎心脏发育multiome数据,解析了免疫细胞亚群及发育阶段的细胞类型特异性染色质互作,并基于预测的染色质环将GWAS非编码变异系统性关联至候选靶基因。
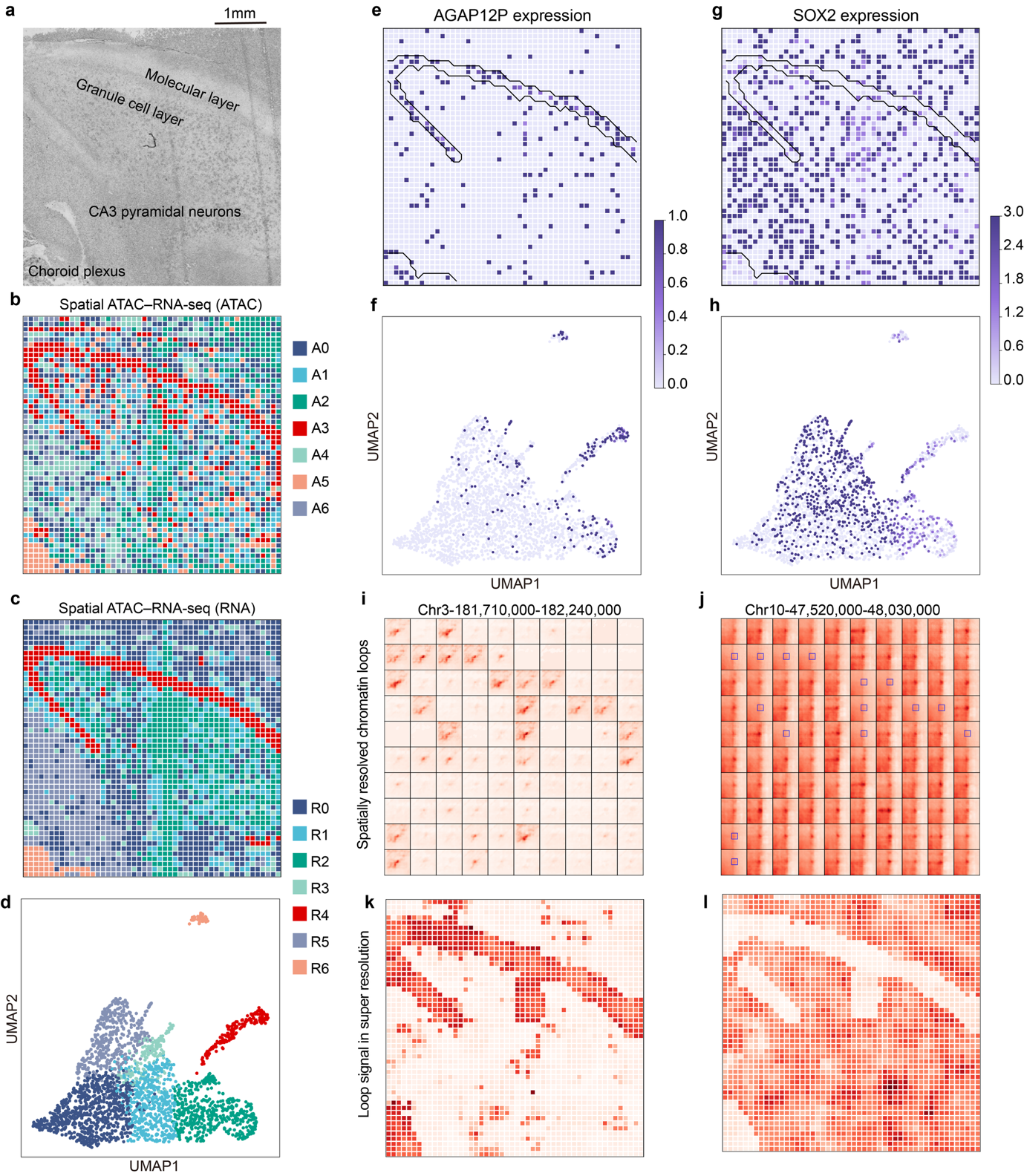
在空间尺度上,作者将框架接入spatial ATAC-seq数据,在人类海马组织中实现了空间分辨的染色质互作预测。此外,作者还通过fine-tuning展示了Hi-Compass的跨物种应用能力。
综上,Hi-Compass提供了一个覆盖bulk—单细胞—空间多尺度、支持跨物种应用的细胞类型特异性三维基因组预测框架,为三维基因组学在发育、免疫、神经及疾病研究中的应用提供了新的工具。
本论文的共同通讯作者为北京大学临床医学高等研究院(细胞稳态与衰老性重大疾病北京研究中心)/北京大学肿瘤医院吴华君研究员、北京大学第三医院徐明教授和北京大学肿瘤医院王玉娟博士;北京大学肿瘤医院孙源辰、北京大学第三医院蒋文杰和北京大学肿瘤医院蔡康文为本文的共同第一作者。
作 者 简 介:
l 吴华君 研究员,博士生导师 现任北京大学临床医学高等研究院/北京大学肿瘤医院助理教授。 主要研究领域为计算基因组学与三维基因组学,聚焦于利用计算方法解析染色质空间结构及其在基因调控和疾病中的功能。
l 徐明 博雅特聘教授, 博士生导师 北京大学研究生院副院长。 主要研究领域为心血管疾病的分子机制与基因组调控研究。
l 王玉娟 博士 。主要研究领域为肿瘤表观遗传与基因调控。
l 孙源辰 硕士,北京大学肿瘤医院技术员。本文共同第一作者。主要研究方向为生物统计学与深度学习在三维基因组中的应用。
l 蒋文杰 北京大学第三医院在读博士研究生。本文共同第一作者。主要研究方向为计算基因组学与三维基因组学。
l 蔡康文 硕士,北京大学肿瘤医院技术员。本文共同第一作者。主要研究方向为生物信息学与深度学习在三维基因组中的应用。
文章链接:https://www.nature.com/articles/s41467-026-71877-z
References
1. Bonev B, Cavalli G. Organization and function of the 3D genome. Nature Reviews Genetics 2016, 17:661–678.
2. Dekker J, Mirny L. The 3D genome as moderator of chromosomal communication. Cell 2016, 164:1110–1121.
3. Hafner A, Boettiger A. The spatial organization of transcriptional control. Nature Reviews Genetics 2023, 24:53–68.
4. Lieberman-Aiden E, et al. Comprehensive mapping of long-range interactions reveals folding principles of the human genome. Science 2009, 326:289–293.
5. Rao SSP, et al. A 3D map of the human genome at kilobase resolution reveals principles of chromatin looping. Cell 2014, 159:1665–1680.
